Naast de hoofdelementen stikstof, kalium en fosfor (de NPK’s) heeft het gewas, in mindere mate, ook sporenelementen nodig in het voedingsschema. De doseringen voor sporenelementen worden in micromol per liter uitgedrukt, een factor 1000 kleiner dan millimol, waarmee we de NPK’s doseren.
Voorbeelden van zulke sporenelementen zijn mangaan, zink, borium, koper en molybdeen. IJzer wordt vaak los genoemd van de andere sporenelementen (sporen en ijzers), maar dit is ook een spoorelement.
Sporenelementen hebben vaak een enzymatische werking. Dat wil zeggen dat ze een rol spelen in de omzetting van bijvoorbeeld nitraten naar eiwitten. Vooral molybdeen speelt hier een belangrijke rol.
Op deze pagina zie je wat er met het gewas gebeurt op het moment dat het één van de sporenelementen mist. Zo zie je bijvoorbeeld dat er bij zinkgebrek vergeling tussen de nerven plaatsvindt en dat er groeiachterstand ontstaat. Het is dus van belang om alle sporenelementen op pijl te houden.
Sporenelementen kunnen op verschillende manieren aan het gewas worden toegediend. Mangaan, zink en koper kunnen worden gekoppeld aan een sulfaat of gekoppeld aan een (EDTA-)chelaat. Op deze manier is het voor het gewas mogelijk om de sporen op te nemen. Ook is het mogelijk om deze elementen gekoppeld aan nitraat toe te dienen. Dit gebeurd in de praktijk echter zelden.
Vanwege de kostprijs hebben sulfaten vaak de voorkeur boven chelaten. Bij een hoge hoeveelheid calcium in het water of een hoge pH in de bodem of het substraat, kan het echter gebeuren dat het sulfaat neerslaat. Het spoorelement kan dan niet worden opgenomen door de plant. Om dit te voorkomen kan ervoor gekozen worden om chelaten te gebruiken in plaats van sulfaten. Ook kunnen chelaten helpen bij de opname van sporenelementen als er sprake is van een hoge pH. Dan worden de sporenelementen namelijk moeilijker opneembaar. Bij chelaatsporen zitten de ionen een soort van ingepakt, de plant kan deze dan uitpakken om ze vervolgens op te nemen. Resultaat is dan een betere sporenopname. Tot slot is een voordeel van chelaten over sulfaten dat de onderlinge concurrentie van mangaan, zink en koper met het ijzerchelaat veel minder is.
Borium en molybdeen kunnen niet gebonden worden aan een chelaat. Hier wordt vaker gekeken naar de inbreng met natrium. Molybdeen kan ook met ammonium worden gebonden. Dit geeft een natriumvrije manier om molybdeen toe te dienen. Deze variant heeft daarnaast ook een hogere concentratie aan molybdeen dan de variant met natrium.
Borium kan als boorzuur worden toegediend. Ook dit is natriumvrij. Het voordeel hiervan is dat er geen natrium wordt ingebracht en dit niet kan stapelen in het substraat of drainwater.
IJzers worden altijd in chelaten toegediend. Het ijzer-ion is namelijk niet sterk genoeg om aan het sulfaat gebonden te blijven en zal oxideren waardoor het niet bij het gewas aankomt. Geoxideerd ijzer kennen we beter als roest. Chelaten werken als een soort molecuulklauwen die het ion vasthouden. Op het moment dat het chelaat met het ijzer-ion bij de wortel aankomt, vindt er een uitwisseling plaats van elementen. Het ijzer komt dan vrij en wordt opneembaar voor de wortel. Een ander element neemt dat de plek van ijzer over in het chelaat.
IJzer in chelaten kan niet alleen in de bodem worden toegepast, maar ook als bladmeststof worden toegepast. Bladbemesting komt in de plant via de huidmondjes (stomate), de bladharen (trichomen), de waslaag op het blad (cuticula) of via het celmembraan (endocytose). De weg die het ijzer uiteindelijk neemt is afhankelijk van de andere componenten van de meststof waar het ijzer in verwerkt zit. Vaak worden zeewierextracten en aminozuren toegevoegd ter bevordering van de opname.
Er zijn verschillende chelaten die elk hun optimale omstandigheden kennen.
EDTA:
Dit chelaat is toepasbaar in een teelt waar de pH niet boven de 6 uitkomt. Wanneer de pH hoger is dan 6 laat dit chelaat het ijzerion los waardoor het ion oxideert en niet wordt opgenomen door het gewas.
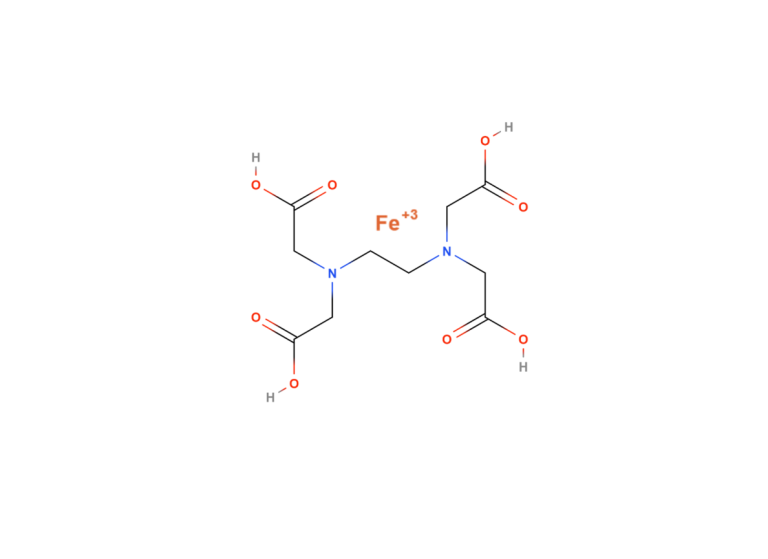
DTPA:
DTPA is het meest toegepaste chelaat in de tuinbouw. Dit chelaat is toepasbaar tot een pH van 7. Een DTPA chelaat is er in een ijzergehalte van 3% en 6%. Het grote verschil zit hem in de opbouw van het chelaat. Bij een ijzergehalte van 3% is het chelaat op basis van natrium. Hierdoor wordt er dus ook direct natrium in het gewas gebracht.
Bij het van ijzergehalte 6% is het chelaat op basis van ammonium.
Als de pH van de teelt hoger dan 7 is, kan je rood ijzer doseren. Rood ijzer is een poeder waarbij de beschikbaarheid tot een pH van 10 goed blijft. Ook rood ijzer is er in verschillende typen:

EDDHA:
Dit is de meest bekende vorm van rood ijzer. EDDHA heeft een ijzergehalte van 6%. Niet de volledige 6% is stabiel. 4 of 4,8% is stabiel, het restant is minder stabiel. Dat wil zeggen dat het ijzer uit het chelaat valt en zal oxideren. EDDHA-chelaat is, net als DPTA 3%, hoofdzakelijk op een natriumchelaat gebaseerd. Hierdoor breng je dus ook een hoeveelheid natrium in de teelt.
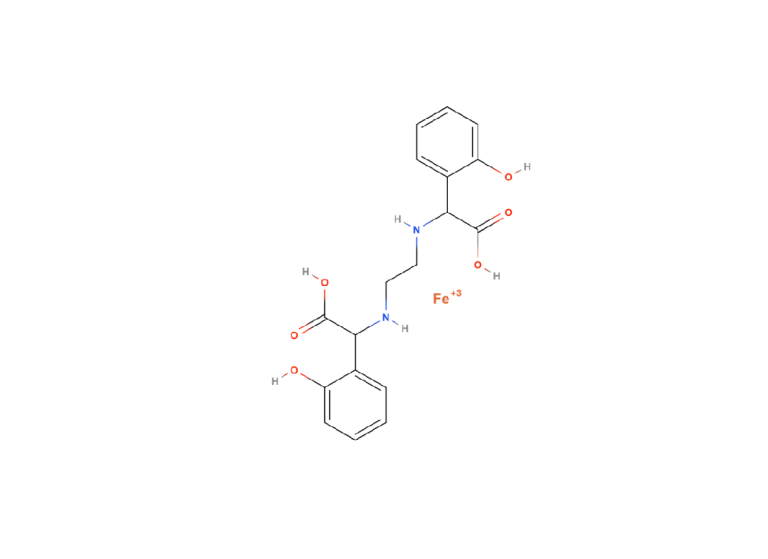
HBED:
Dit is een meer stabiel rood ijzer. Hier blijft dus de gehele 6% van het ijzer in de chelaten aanwezig en dus beschikbaar voor het gewas. Je hebt hierdoor voor dezelfde hoeveelheid ijzer dus minder product nodig dan van EDDHA. HBED is een chelaat op basis van kalium.
